來自星星的你﹕淺談自閉症與EMBP治療
自閉症的功能障礙
 |
 |
 |
自閉症譜系障礙(Autism Spectrum Disorders, ASD)有三個主要項目:典型自閉症(Classic autism)、亞斯伯格症候群(Asperger syndrome)、待分類的廣泛性發展障礙(Pervasive Developmental Disorder Not Otherwise Specified, PDD-NOS)。自閉症在光譜核心位置,亞斯伯格症候群最接近自閉症之處在於徵狀及相似的成因,而與自閉症者不同在於語言發展並未出現遲緩。廣泛性發展障礙,亦作非典型自閉症,泛指一般有自閉症傾向,但不能透過其特徵而歸類為更具體的分類,佔了自閉症光譜的90%。自閉症是一種神經行為症候群,中樞神經系統產生功能障礙,擾亂腦部活動發展。2013年DSM–5(《精神疾病診斷與統計手冊》第五版)將原本常見自閉症名稱(Autism)調整為自閉症譜系障礙(Autism Spectrum Disorder, ASD)。徵狀通常在幼兒三歲前出現,常伴隨有智障、癲癇、過度活躍、退縮及鬧情緒等問題。患有自閉症的孩子在日常生活中有三大障礙:人際關係障礙、語言表達障礙及行為障礙。
自閉症的發病率
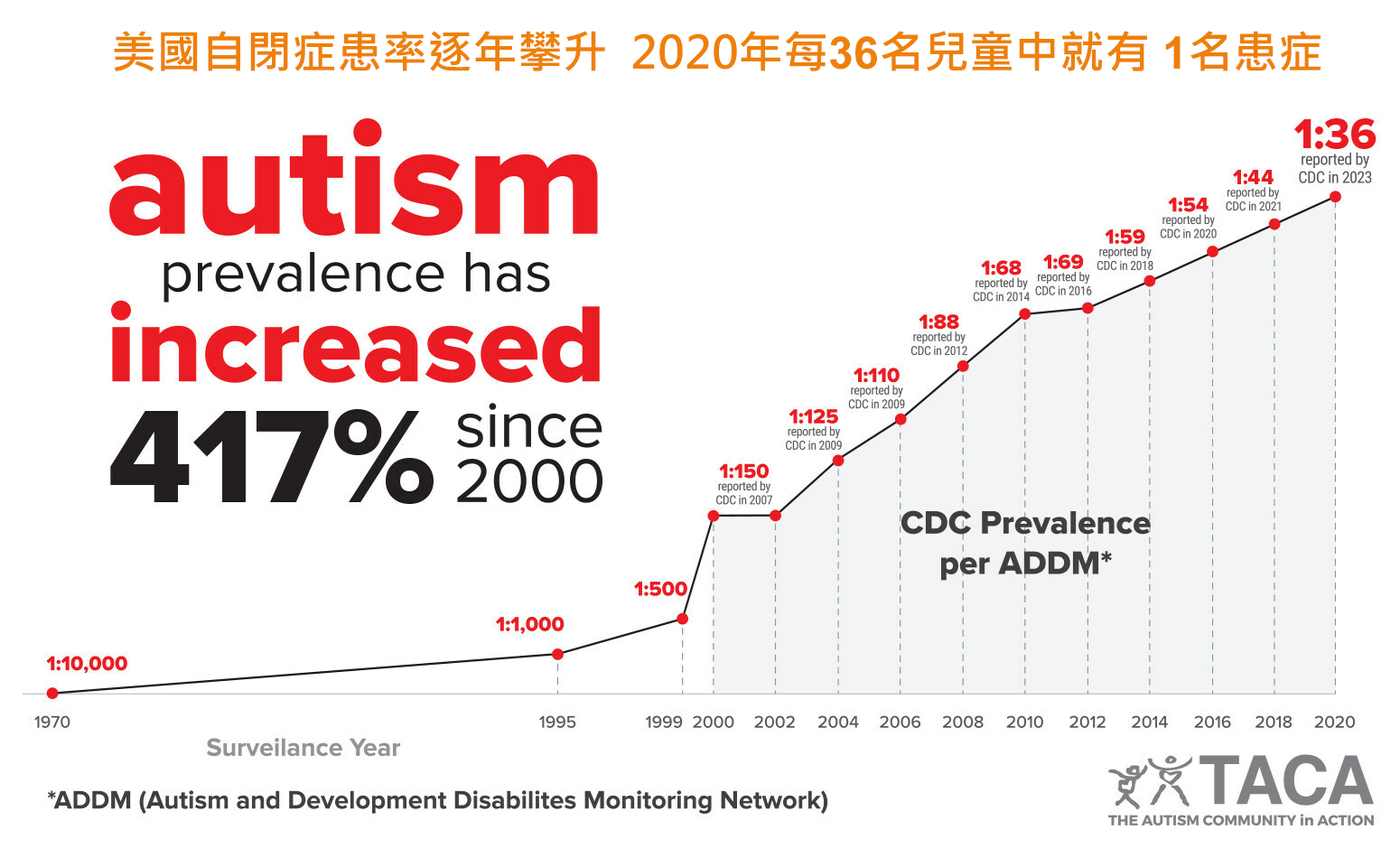
於2006年,來自美國疾病控制和預防中心(CDC)的統計數據,確定約110個美國兒童中有1個屬於自閉症,患病率在過去二十年增長600%。在2022年,CDC發現自閉症的發病率進一步上升達到36個美國兒童中有1個。在16年時間增長了3倍之多。而在台灣每年自閉症患者也是增加的,2022年有1萬7550人。相較10年前,自閉症在10年間增加2.7倍,是身心障礙者中增加幅度最大之一。統計發生率台灣在十萬的人口中約有199個自閉症患者,與歐美國家相比,大約只有1/10,但自閉症並沒有人種的差異,只能說先進國家的診斷率還是比台灣高很多。男生的ASD發生率比女生高出4至5倍,為什麼男孩比較容易有自閉症,目前無確定的原因。
自閉症的病因
導致自閉症的原因,仍然未有定論。隨著研究的發展,可能的原因可以分為兩大類:基因遺傳和環境。研究顯示,自閉症多達72%是基因遺傳,但其遺傳方式非常複雜,目前也沒有確定的基因和自閉症有絕對關係。環境和外部的影響,亦有可能是造成自閉症的因素,包括: 產前的環境因素,如用藥、高齡產婦、病毒感染等導致出生缺陷。而出生後的環境因素,如兒童的飲食、藥物或者一些重金屬中毒亦有人提及。
而在病理學上則發現到,有些腦部關鍵區域發現神經元過剩,引起細胞間過度連接;妊娠早期神經元遷徙障礙;激動-抑制性神經網絡失衡等。這些變化似乎都與突觸發育受阻有關,而後者又與癲癇發作密切相關。這似乎也解釋了為什麼臨床上自閉症和癲癇常聯繫在一起。
自閉症在定量腦電圖(QEEG)上的發現
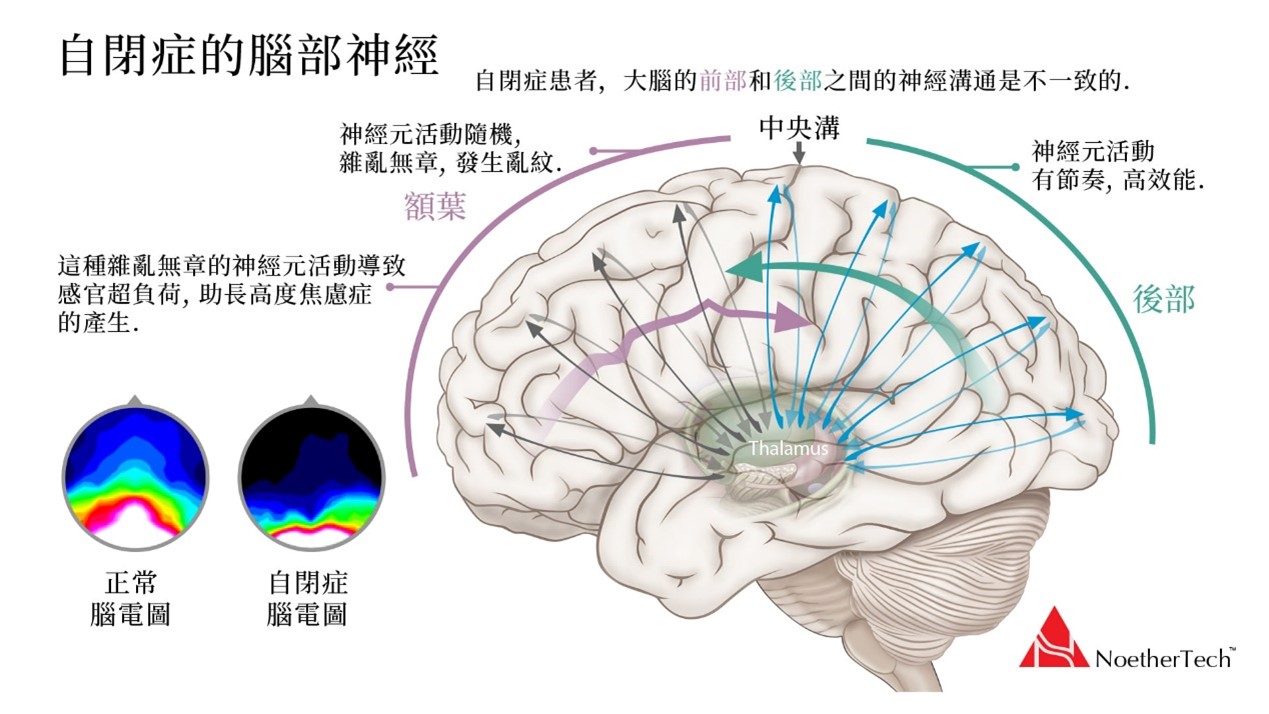
自閉症患者在神經影像學檢測一般看不出明顯的變化,但在功能性成像技術則多半顯示額葉皮層糖代謝增加和局部血流灌注增加。腦電生理學研究常可發現與癲癇有關的異常放電。除此而外,也有實驗發現兒童自閉症患者有比正常對照兒童高得多的高頻γ活動。而其增高的程度與發育遲緩的嚴重度成正比。而在我們的臨床工作和研究中也發現有類似的現象,除了局灶性棘慢波,最突出的腦電變化是α波功率和節律性降低,高頻、不規則波增加,特別是在額葉的部分。
EMBP健柏診所對於自閉症的觀點
從腦波的角度來看,自閉症患者規整的α功率和節律性降低,不規整的其他頻率,尤其是高頻β、γ活動增加。我們可以想像得出來當大腦節律性活動出現異常時,神經元隨機放電增加,能量代謝為之提高,產熱增加。這種系統的高能量狀態是不穩定的,我們把這種情況稱之為「大腦的內在性焦慮」。在這種情況之下,個體必須做出行為的代償來幫助降低耗能以提高系統穩定性。
所以自閉症患者原發的社交障礙和其他減少信號攝入的行為,例如避免對視、重覆言行等。這些「主動」減少信號的做法在客觀上補償了腦內神經活動節律性的降低,限制了由外界信號導致的代謝增量,避免大腦過載。同時,由於腦內節律性「時鐘」的紊亂,神經信號無法正確編碼,因而導致信號錯解,出現幻覺、妄想、多種無法解釋的軀體不適等臨床症狀。如果自閉症治療僅著眼於行為糾正,而不去關注症狀背後的神經機制,未免有捨本求末之虞。 總體而言,自閉症被認為是一種神經發育障礙,這種障礙延遲而且中斷正常認知發展和表達。而主因則為每一個自閉症孩子的大腦神經傳達不佳,而造成患者產生壓倒性、癱瘓感覺的焦慮。而EMBP則提供了解決「大腦的內在性焦慮」的最好方法。
EMBP治療自閉症
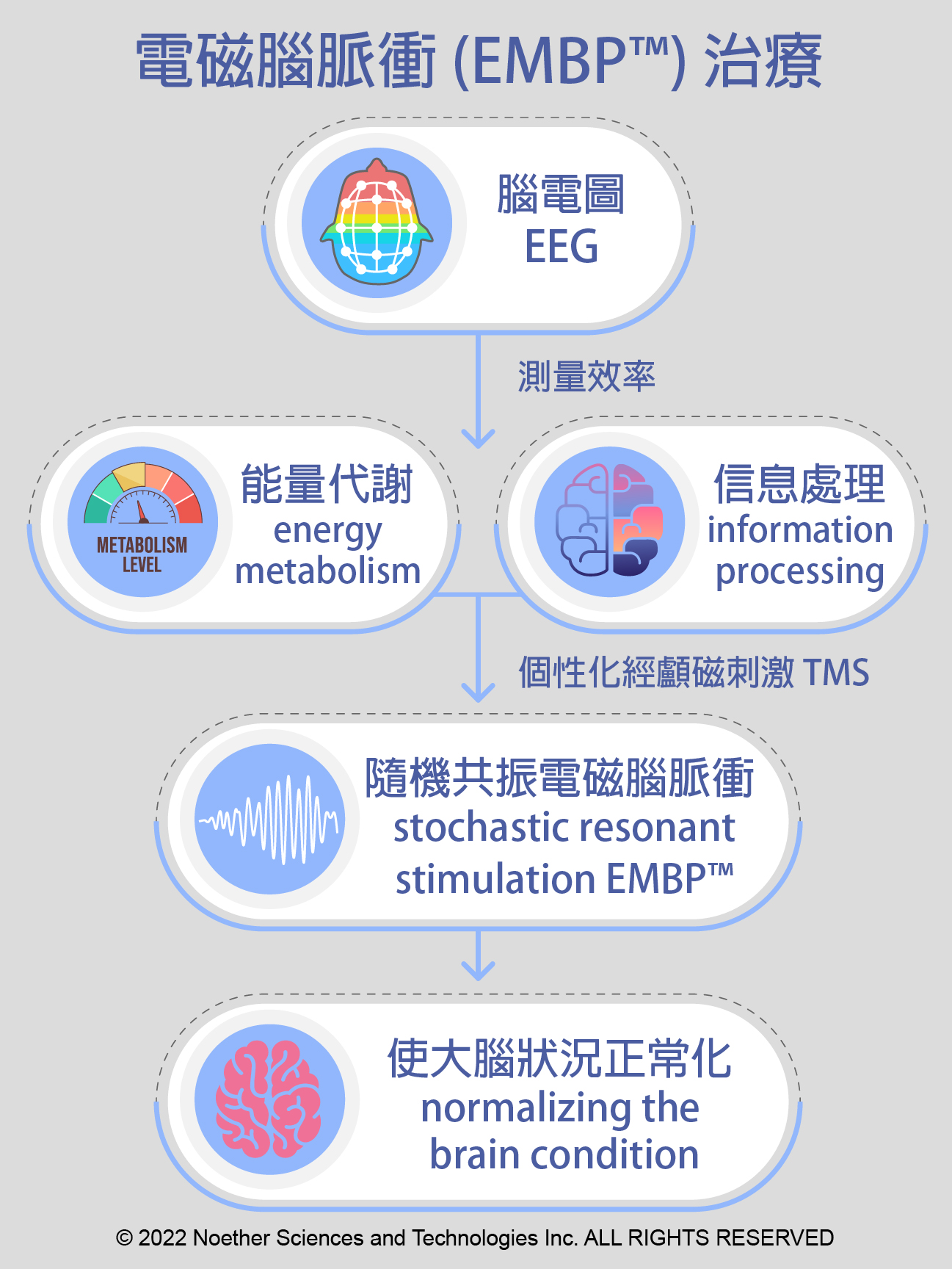
在我們的觀念之中,不論病人的診斷、症狀表現為何,其根本的問題是大腦神經元之間無法有效率的運作,而我們認為每位自閉症病患都應該接受個人化的療法與治療程序。而EMBP結合了定量腦電圖以及經顱磁刺激術,經過獨特的大數據運算模式,能夠針對病患的大腦如何接收、處理並傳達資訊提供高度個人化的治療方式。如此的治療能確保照護品質與計畫符合醫療標準,確保個人大腦相關的一致性。透過EMBP能夠緩和自閉症所引起的焦慮、感官超載、感覺處理、過渡困難、挑食、情緒崩潰等因為大腦能量狀態過高而無法負荷的症狀。
EMBP治療實例分享
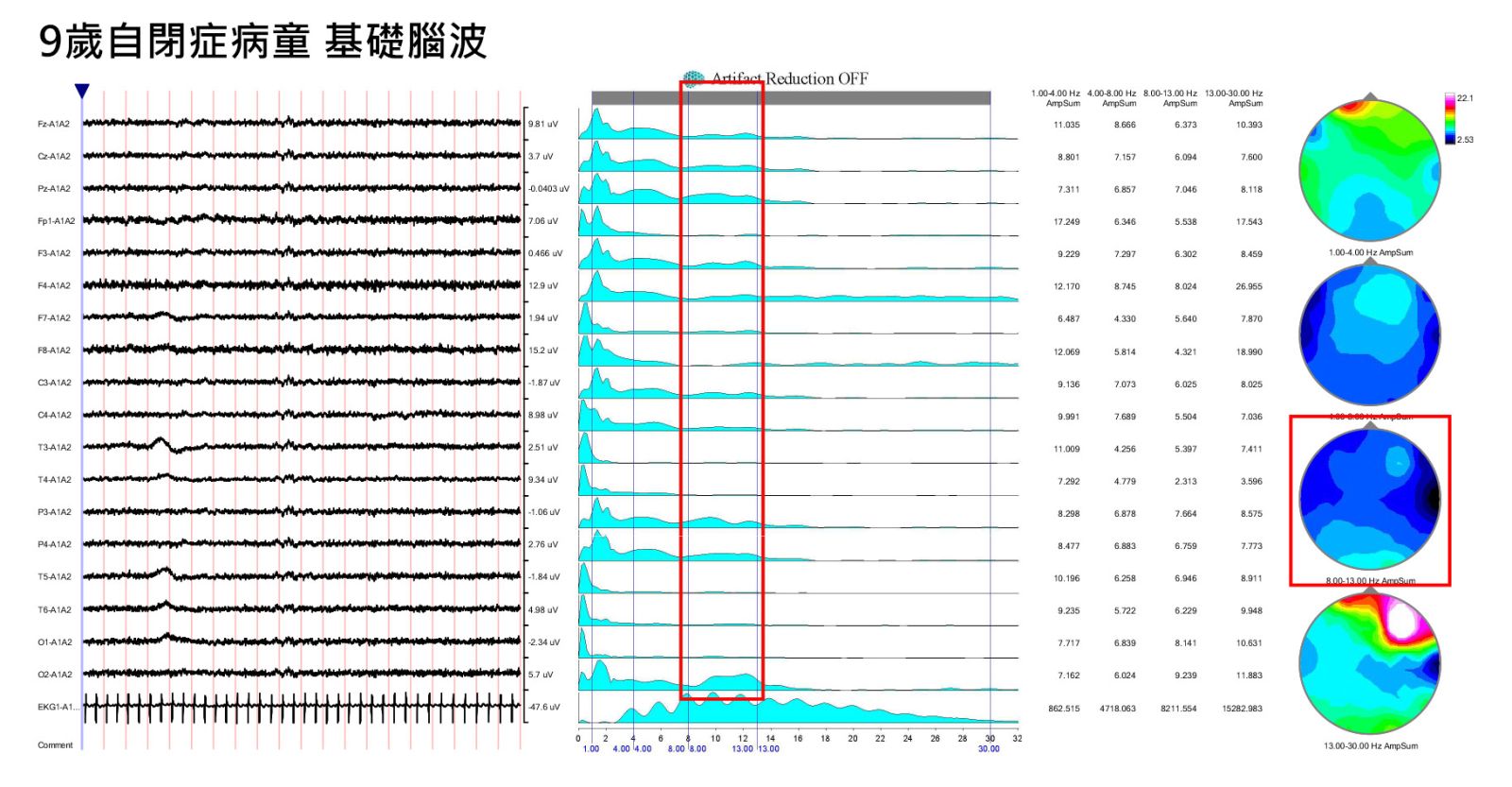
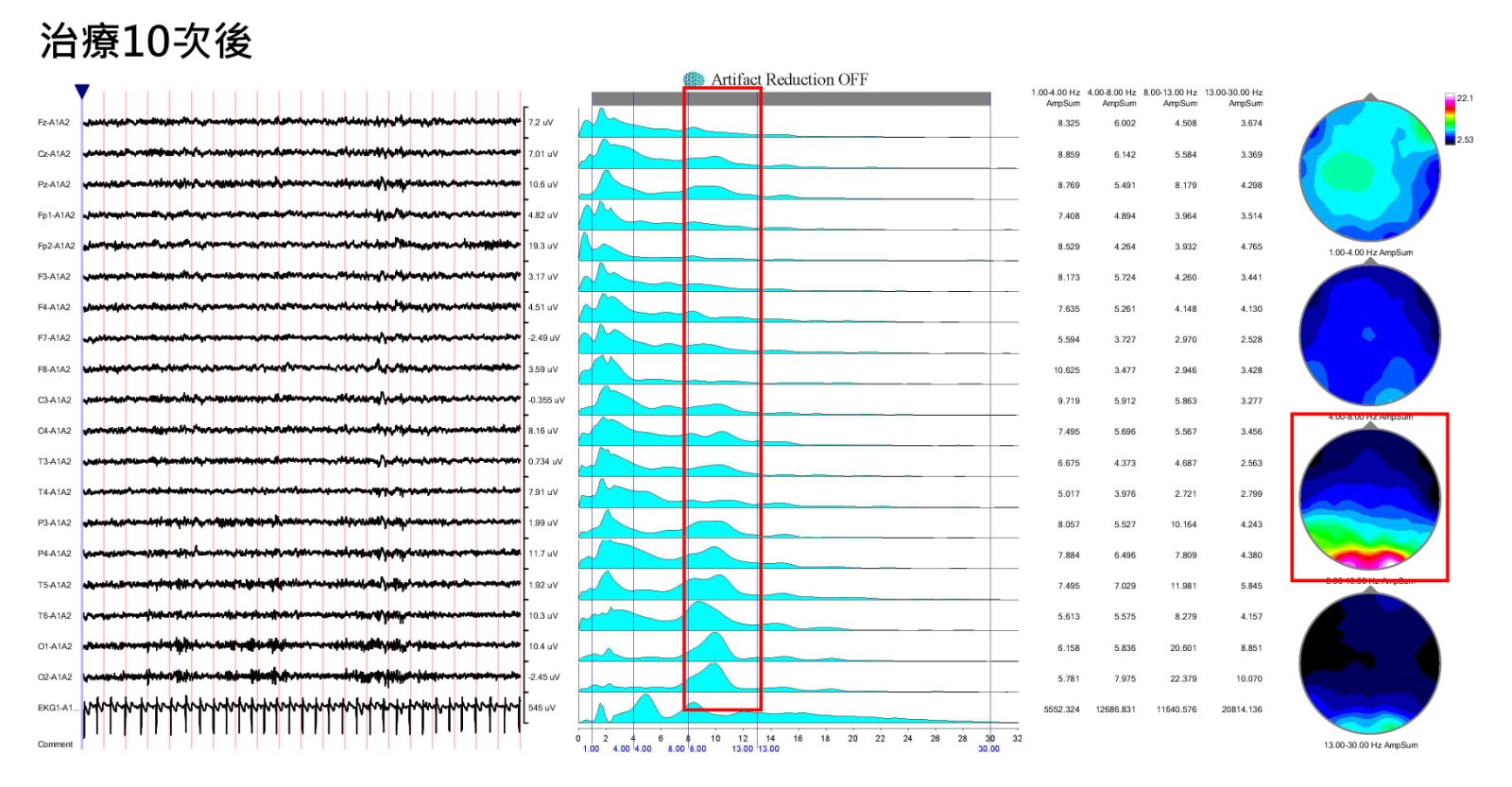
起初因為孩子沒有辦法很配合,我們盡量安撫他,那在比較平靜的時候我們可以取得較好的腦波片段,可以發現在孩子的大腦之中(紅框部分),幾乎都是分散的Alpha波,整個大腦信息訊號凌亂不堪。在這種情況下,孩子的大腦光是要應付訊息傳遞都沒辦法了,自然而然就呈現焦慮的狀態。在經過十次治療之後,孩子比較能配合檢查,我們也發現大腦裡開始出現統整性的信號。腦內的內在性焦慮降低了,外顯症狀自然能夠穩定得多,比如情緒上相對能平靜下來,或者家長也能發現一些指令更能清晰地接收。這樣的進展是我們所期待的,之後也才能慢慢調整大腦其餘的問題。
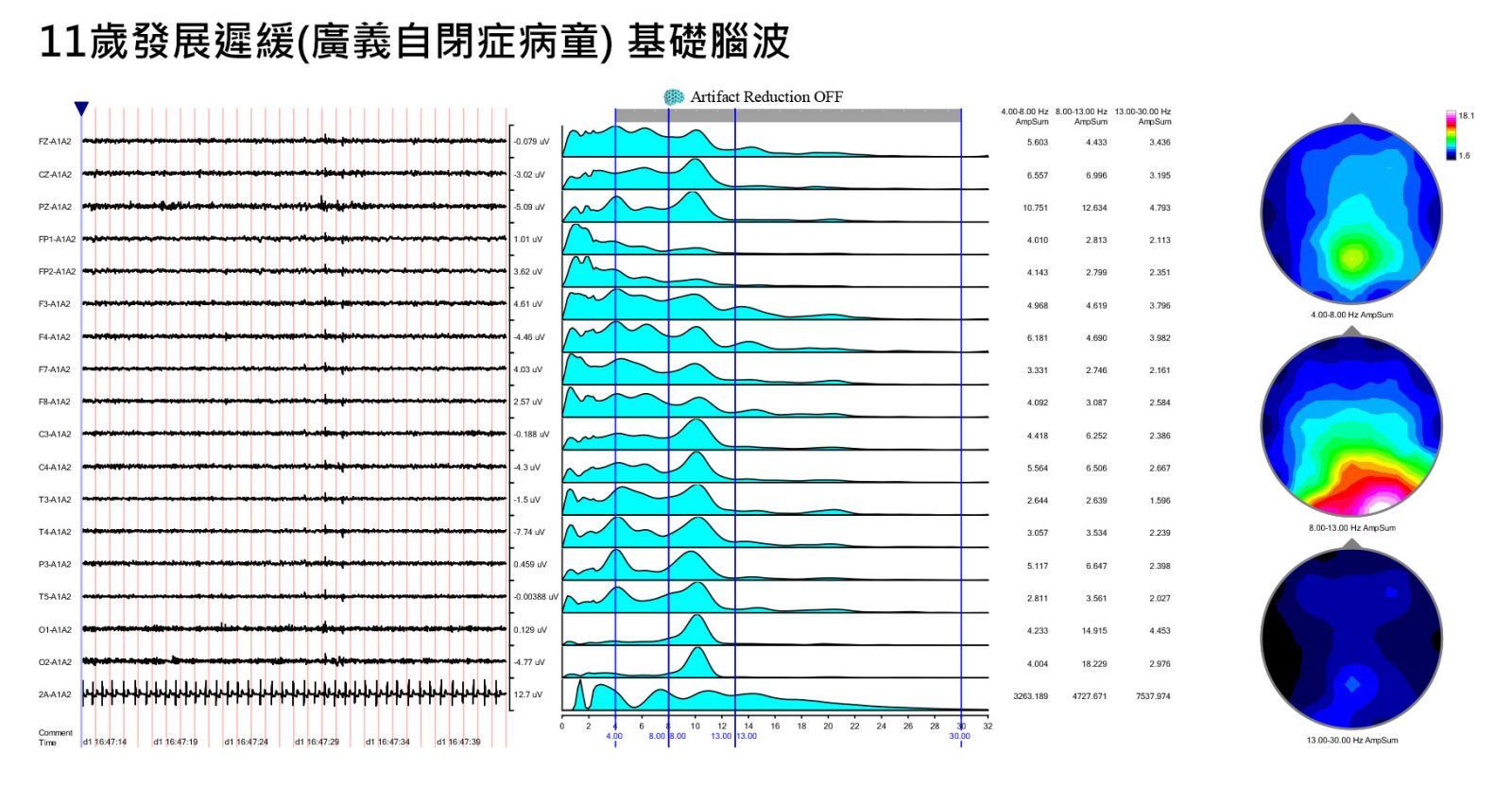
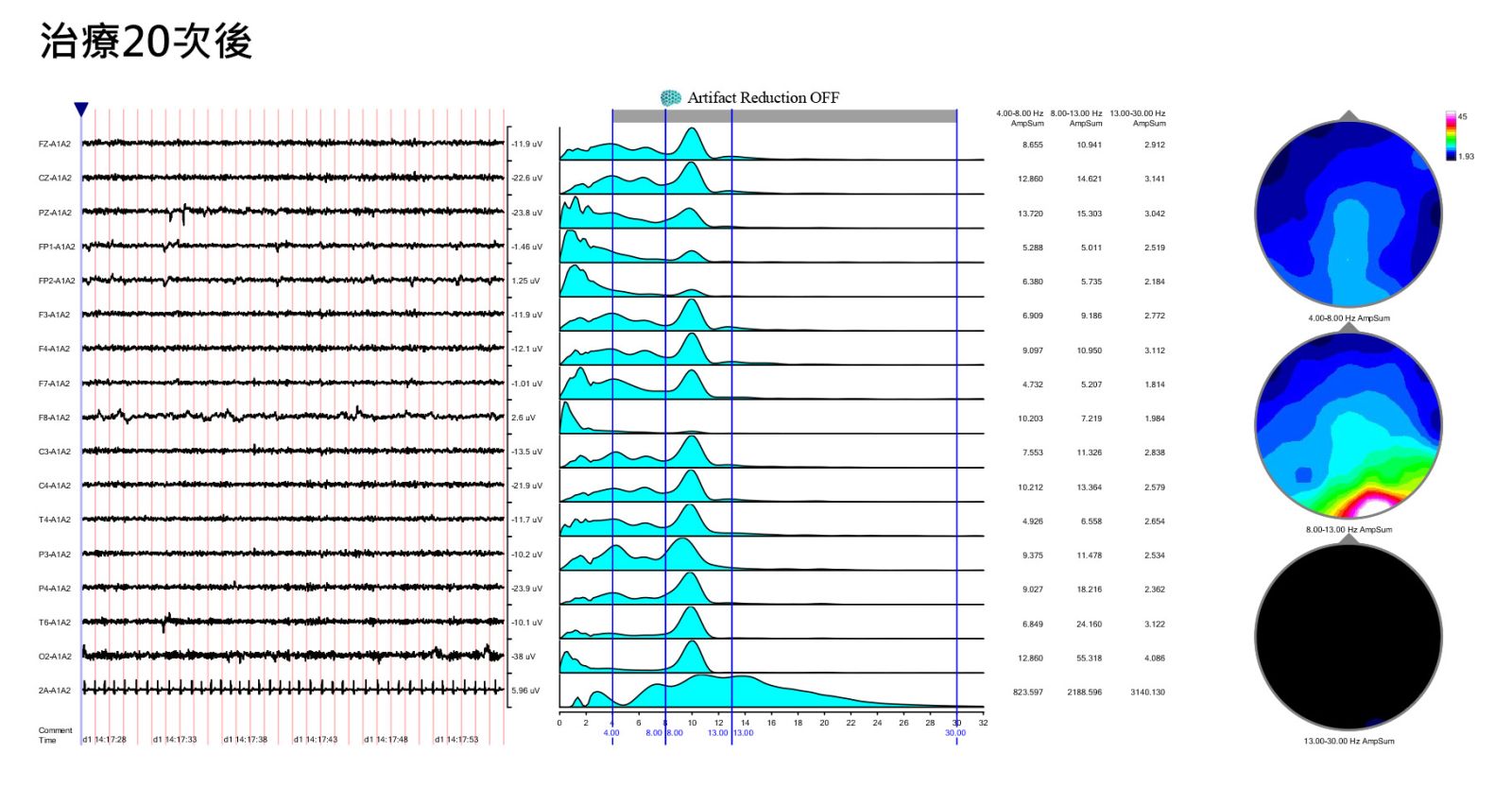
我們可以明顯看到大腦內4-8Hz的Theta慢波變少了,而整個節律性的正常Alpha波提升,代表大腦中訊號及能量代謝穩定。家長的回饋發現到孩子的整體睡眠品質提升,學習力也提高了。
參考文獻
- 金怡(2011): 意識現象與熱力學, 北京大學醫學出版社
- Matthew J. Maenner; Zachary Warren: Prevalence and Characteristics of Autism Spectrum Disorder Among Children Aged 8 Years — Autism and Developmental Disabilities Monitoring Network, 11 Sites, United States, 2020. Surveillance Summaries / March 24, 2023 / 72(2);1–14.
- Eric Courchesne, Karen Pierce, Cynthia M Schumann: Mapping early brain development in autism. Neuron. 2007 Oct 25; 56(2):399-413. Antonio M Persico, Thomas Bourgeron: Searching for ways out of the autism maze: genetic, epigenetic and environmental clues. Trends Neuroscience 2006 Jul;29(7):349-358.
- Sam Wass: Distortions and disconnections: Disrupted brain connectivity in autism. Brain and Cognition 2011 Feb; 75(1):18-28.
- Patricia M Villemagne, Sakkubai Naidu, Victor L Villemagne: Brain glucose metabolism in Rett Syndrome. Pediatr Neurol. 2002 Aug;27(2):117-22.
- Elena V Orekhova, Tatiana A Stroganova: Excess of high frequency electroencephalogram oscillations in boys with autism. Biol Psychiatry. 2007 Nov 1;62(9):1022-9.
自閉症的功能障礙
 |
 |
 |
自閉症譜系障礙(Autism Spectrum Disorders, ASD)有三個主要項目:典型自閉症(Classic autism)、亞斯伯格症候群(Asperger syndrome)、待分類的廣泛性發展障礙(Pervasive Developmental Disorder Not Otherwise Specified, PDD-NOS)。自閉症在光譜核心位置,亞斯伯格症候群最接近自閉症之處在於徵狀及相似的成因,而與自閉症者不同在於語言發展並未出現遲緩。廣泛性發展障礙,亦作非典型自閉症,泛指一般有自閉症傾向,但不能透過其特徵而歸類為更具體的分類,佔了自閉症光譜的90%。自閉症是一種神經行為症候群,中樞神經系統產生功能障礙,擾亂腦部活動發展。2013年DSM–5(《精神疾病診斷與統計手冊》第五版)將原本常見自閉症名稱(Autism)調整為自閉症譜系障礙(Autism Spectrum Disorder, ASD)。徵狀通常在幼兒三歲前出現,常伴隨有智障、癲癇、過度活躍、退縮及鬧情緒等問題。患有自閉症的孩子在日常生活中有三大障礙:人際關係障礙、語言表達障礙及行為障礙。
自閉症的發病率

於2006年,來自美國疾病控制和預防中心(CDC)的統計數據,確定約110個美國兒童中有1個屬於自閉症,患病率在過去二十年增長600%。在2022年,CDC發現自閉症的發病率進一步上升達到36個美國兒童中有1個。在16年時間增長了3倍之多。而在台灣每年自閉症患者也是增加的,2022年有1萬7550人。相較10年前,自閉症在10年間增加2.7倍,是身心障礙者中增加幅度最大之一。統計發生率台灣在十萬的人口中約有199個自閉症患者,與歐美國家相比,大約只有1/10,但自閉症並沒有人種的差異,只能說先進國家的診斷率還是比台灣高很多。男生的ASD發生率比女生高出4至5倍,為什麼男孩比較容易有自閉症,目前無確定的原因。
自閉症的病因
導致自閉症的原因,仍然未有定論。隨著研究的發展,可能的原因可以分為兩大類:基因遺傳和環境。研究顯示,自閉症多達72%是基因遺傳,但其遺傳方式非常複雜,目前也沒有確定的基因和自閉症有絕對關係。環境和外部的影響,亦有可能是造成自閉症的因素,包括: 產前的環境因素,如用藥、高齡產婦、病毒感染等導致出生缺陷。而出生後的環境因素,如兒童的飲食、藥物或者一些重金屬中毒亦有人提及。
而在病理學上則發現到,有些腦部關鍵區域發現神經元過剩,引起細胞間過度連接;妊娠早期神經元遷徙障礙;激動-抑制性神經網絡失衡等。這些變化似乎都與突觸發育受阻有關,而後者又與癲癇發作密切相關。這似乎也解釋了為什麼臨床上自閉症和癲癇常聯繫在一起。
自閉症在定量腦電圖(QEEG)上的發現

自閉症患者在神經影像學檢測一般看不出明顯的變化,但在功能性成像技術則多半顯示額葉皮層糖代謝增加和局部血流灌注增加。腦電生理學研究常可發現與癲癇有關的異常放電。除此而外,也有實驗發現兒童自閉症患者有比正常對照兒童高得多的高頻γ活動。而其增高的程度與發育遲緩的嚴重度成正比。而在我們的臨床工作和研究中也發現有類似的現象,除了局灶性棘慢波,最突出的腦電變化是α波功率和節律性降低,高頻、不規則波增加,特別是在額葉的部分。
EMBP健柏診所對於自閉症的觀點
從腦波的角度來看,自閉症患者規整的α功率和節律性降低,不規整的其他頻率,尤其是高頻β、γ活動增加。我們可以想像得出來當大腦節律性活動出現異常時,神經元隨機放電增加,能量代謝為之提高,產熱增加。這種系統的高能量狀態是不穩定的,我們把這種情況稱之為「大腦的內在性焦慮」。在這種情況之下,個體必須做出行為的代償來幫助降低耗能以提高系統穩定性。
所以自閉症患者原發的社交障礙和其他減少信號攝入的行為,例如避免對視、重覆言行等。這些「主動」減少信號的做法在客觀上補償了腦內神經活動節律性的降低,限制了由外界信號導致的代謝增量,避免大腦過載。同時,由於腦內節律性「時鐘」的紊亂,神經信號無法正確編碼,因而導致信號錯解,出現幻覺、妄想、多種無法解釋的軀體不適等臨床症狀。如果自閉症治療僅著眼於行為糾正,而不去關注症狀背後的神經機制,未免有捨本求末之虞。 總體而言,自閉症被認為是一種神經發育障礙,這種障礙延遲而且中斷正常認知發展和表達。而主因則為每一個自閉症孩子的大腦神經傳達不佳,而造成患者產生壓倒性、癱瘓感覺的焦慮。而EMBP則提供了解決「大腦的內在性焦慮」的最好方法。
EMBP治療自閉症
在我們的觀念之中,不論病人的診斷、症狀表現為何,其根本的問題是大腦神經元之間無法有效率的運作,而我們認為每位自閉症病患都應該接受個人化的療法與治療程序。而EMBP結合了定量腦電圖以及經顱磁刺激術,經過獨特的大數據運算模式,能夠針對病患的大腦如何接收、處理並傳達資訊提供高度個人化的治療方式。如此的治療能確保照護品質與計畫符合醫療標準,確保個人大腦相關的一致性。透過EMBP能夠緩和自閉症所引起的焦慮、感官超載、感覺處理、過渡困難、挑食、情緒崩潰等因為大腦能量狀態過高而無法負荷的症狀。

EMBP治療實例分享


起初因為孩子沒有辦法很配合,我們盡量安撫他,那在比較平靜的時候我們可以取得較好的腦波片段,可以發現在孩子的大腦之中(紅框部分),幾乎都是分散的Alpha波,整個大腦信息訊號凌亂不堪。在這種情況下,孩子的大腦光是要應付訊息傳遞都沒辦法了,自然而然就呈現焦慮的狀態。在經過十次治療之後,孩子比較能配合檢查,我們也發現大腦裡開始出現統整性的信號。腦內的內在性焦慮降低了,外顯症狀自然能夠穩定得多,比如情緒上相對能平靜下來,或者家長也能發現一些指令更能清晰地接收。這樣的進展是我們所期待的,之後也才能慢慢調整大腦其餘的問題。


我們可以明顯看到大腦內4-8Hz的Theta慢波變少了,而整個節律性的正常Alpha波提升,代表大腦中訊號及能量代謝穩定。家長的回饋發現到孩子的整體睡眠品質提升,學習力也提高了。
參考文獻
- 金怡(2011): 意識現象與熱力學, 北京大學醫學出版社
- Matthew J. Maenner; Zachary Warren: Prevalence and Characteristics of Autism Spectrum Disorder Among Children Aged 8 Years — Autism and Developmental Disabilities Monitoring Network, 11 Sites, United States, 2020. Surveillance Summaries / March 24, 2023 / 72(2);1–14.
- Eric Courchesne, Karen Pierce, Cynthia M Schumann: Mapping early brain development in autism. Neuron. 2007 Oct 25; 56(2):399-413. Antonio M Persico, Thomas Bourgeron: Searching for ways out of the autism maze: genetic, epigenetic and environmental clues. Trends Neuroscience 2006 Jul;29(7):349-358.
- Sam Wass: Distortions and disconnections: Disrupted brain connectivity in autism. Brain and Cognition 2011 Feb; 75(1):18-28.
- Patricia M Villemagne, Sakkubai Naidu, Victor L Villemagne: Brain glucose metabolism in Rett Syndrome. Pediatr Neurol. 2002 Aug;27(2):117-22.
- Elena V Orekhova, Tatiana A Stroganova: Excess of high frequency electroencephalogram oscillations in boys with autism. Biol Psychiatry. 2007 Nov 1;62(9):1022-9.
